Ученые обнаружили молекулярный механизм, который помогает опухоли вырабатывать устойчивость к химиопрепаратам. Он включается в качестве резервного варианта при отсутствии гена р53, который в норме помогает предотвращать мутации в здоровых клетках. Около половины опухолей не имеют р53.
Обнаруженный резервный механизм называется MK2. Он помогает клеткам восстанавливать поврежденную ДНК, не вызывая, в отличии от р53, их гибель. Таким образом, если клетка содержит поврежденную ДНК, не подлежащую ремонту, она продолжает делиться.
Химиопрепараты повреждают ДНК клетки и останавливают ее деление. Но при отсутствии р53 раковые клетки продолжают делиться, благодаря MK2. Опухоль продолжает расти, несмотря на химиотерапию.
Исследователи из Массачусетского технологического института в Кембридже (Massachusetts Institute of Technology in Cambridge) рассказывают в журнале Cancer Cell о том, что они обнаружили ключевое вещество в этом сигнальном пути – РНК-связывающий белок hnRNPA0. Старший автор исследования, профессор биологии и биологической инженерии Майкл Яффе (Michael Yaffe), объясняет:
«Я считаю, что этот РНК-связывающий белок – именно то, что делает опухолевые клетки, лишенные р53, устойчивыми к химиотерапии».
В здоровых клетках р53 контролирует деление и «выключает» его, если ДНК повреждена. А при сильном повреждении ДНК запускается апоптоз – программируемая клеточная гибель.
Профессор Яффе с коллегами обнаружили, что при отсутствии р53, – что характерно для половины всех опухолей, – его функции берет на себя механизм MK2. Создав препараты для таргетной терапии, направленные на этот резервный путь, можно будет существенно повысить чувствительность рака к химиопрепаратам.
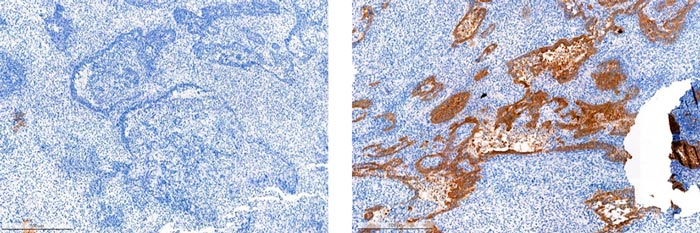
Отсутствие экспрессии p53 слева и выраженная экспрессия p53 справа
Кроме того, ученые считают, что, определяя в клетках больного р53 и MK2, можно будет предсказать, как он будет реагировать на химиотерапию. Это предположение было подтверждено в ходе исследования, в котором приняли участие пациенты, страдающие раком легких II стадии.
Далее, проводя опыты над мышами, ученые оценили, может ли механизм MK2 стать мишенью для таргетной терапии, которая поможет повысить чувствительность опухоли к химиопрепаратам. В частности, исследователи используют особые наногубки, которые «чистят» молекулы РНК-связывающего белка hnRNPA0 и не позволяют ему способствовать выживанию раковых клеток.
Это открытие стало еще одним шагом в развитии персонализированного лечения рака. Каждая опухоль содержит биомаркеры – особые молекулы, которые определяют ее характеристики и реакцию на те или иные химиопрепараты. Благодаря сотрудничеству с американскими лабораториями, в Европейской клинике имеется возможность составлять «молекулярный портрет» опухоли и подбирать наиболее эффективные комбинации препаратов.
Источник: www.medicalnewstoday.com
Читайте также:
круглосуточно
и событий клиники